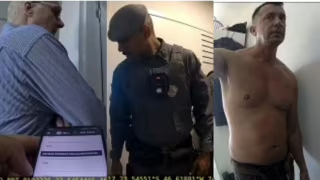
STF: 2ª Turma decide hoje sobre possível liberação da prisão preventiva de Daniel Vorcaro
Em sessão virtual iniciada em 13/03/2026, colegiado avalia se referenda ou revisa decisão individual do ministro André Mendonça no caso ligado ao Banco Master
O fim da patente do Ozempic no Brasil, oficializado nesta sexta-feira (20), abre caminho para versões genéricas e similares do medicamento, mas esses produtos ainda não estão disponíveis nas farmácias. A principal razão é o rigor do processo de aprovação conduzido pela Anvisa, que exige comprovação de eficácia, segurança e qualidade antes da liberação de qualquer novo remédio. Atualmente, a Anvisa recebeu 17 solicitações de registro relacionadas à semaglutida, princípio ativo presente tanto no Ozempic quanto no Wegovy. Veja os próximos passos na Live.
Um levantamento dos pedidos mostra que existem oito processos em análise para novos medicamentos com o mesmo princípio ativo do Ozempic. Entre eles, sete são de origem sintética e um de origem biológica. Outros nove produtos ainda aguardam o início da análise pelas áreas técnicas.
A patente da semaglutida no Brasil expira nesta sexta-feira (20/03), mas, para que qualquer medicamento possa ser oferecido no mercado nacional, é obrigatória a comprovação de eficácia, segurança e qualidade, feita por meio do registro na Anvisa.
A análise dos processos atuais teve início no segundo semestre de 2025, após a publicação de um edital que priorizou a avaliação de produtos análogos do GLP-1, classificação à qual a semaglutida pertence. O primeiro pedido de registro entrou na Anvisa no fim de 2023, mas a maior parte das solicitações chegou apenas no ano passado.
Neste momento, dois pedidos de registro de semaglutida sintética estão em exigência, isto é, dependem da apresentação de dados adicionais pelas empresas para que a avaliação prossiga. Nos dois casos, o prazo para resposta vai até o fim de junho, o que impede a definição de datas para conclusão do processo.
Na área de biológicos, um produto está em análise e outro aguarda o início da avaliação. Já os demais pedidos em andamento devem ter uma posição das áreas técnicas até o fim de abril, seja por aprovação, reprovação ou pela emissão de nova exigência técnica.
A necessidade de informações complementares é comum quando se trata de tecnologias mais complexas. Quanto mais sofisticado o produto, maior tende a ser o volume de dados exigido para demonstrar segurança e eficácia.
Produtos biológicos são medicamentos elaborados a partir de insumo farmacêutico ativo biológico. São moléculas complexas, obtidas a partir de fluidos biológicos, tecidos de origem animal ou procedimentos biotecnológicos, que envolvem manipulação ou inserção de material genético (DNA recombinante) ou alteração de genes.
Nessa categoria estão, por exemplo, vacinas, soros hiperimunes, hemoderivados, anticorpos monoclonais e canetas GLP-1 produzidas por processo biológico. Em geral, esses medicamentos são aplicados por via injetável (endovenosa ou subcutânea) para preservar sua integridade estrutural e funcional, embora também possam ser utilizados por via oral.
Já os medicamentos sintéticos são produzidos por síntese química, resultando em moléculas pequenas e estáveis, que podem ser reproduzidas de forma idêntica. Eles são usados por diversas vias de administração, como oral, injetável, inalatória e oftálmica.
Os chamados análogos sintéticos de biológicos são obtidos por via sintética, mas reproduzem a estrutura de um produto biológico. Por apresentarem características tanto de medicamentos sintéticos quanto de biológicos, são considerados de alta complexidade.
No Brasil, os medicamentos à base de semaglutida já registrados são produtos biológicos. Os novos pedidos em avaliação se dividem em duas categorias: biossimilares, obtidos por via biológica, e sintéticos, produzidos por síntese química. Estes últimos são denominados análogos sintéticos de peptídeos biológicos.
Para medicamentos biológicos, não existe a opção de registro como genéricos. O produto precisa se enquadrar em uma das duas categorias citadas. Eles podem ser avaliados por meio de diversos ensaios de comparação com o biológico de referência, mas não são classificados como genéricos nem similares: são análogos sintéticos de produtos biológicos.
A avaliação desses análogos sintéticos de semaglutida é hoje tratada como um desafio técnico por agências reguladoras em todo o mundo. Até o momento, nenhuma das principais agências de medicamentos, como as do Japão, Europa e Estados Unidos, registrou análogos sintéticos de semaglutida.
Um dos motivos é a necessidade de aplicar, simultaneamente, parâmetros usados para fármacos sintéticos e para biológicos. Esses produtos compartilham características típicas de medicamentos sintéticos, como resíduos de solventes, resíduos de catalisadores metálicos e impurezas com estrutura química semelhante, e, ao mesmo tempo, apresentam riscos típicos de biológicos, como imunogenicidade e formação de agregados.
Para conduzir essa análise, a Anvisa utiliza como referência guias de outras agências internacionais, entre elas o documento da agência dos Estados Unidos, a Food and Drug Administration (FDA), já que ainda não há harmonização global para a avaliação desse tipo de medicamento.
Entre os principais pontos de atenção técnica estão os ensaios de impurezas, a formação de agregados, a garantia de esterilidade e a imunogenicidade. A avaliação busca assegurar, por exemplo, que o medicamento não provoque reações imunes indesejadas.
Um risco monitorado é a criação de anticorpos antifármaco, que pode tornar ineficaz qualquer tratamento com semaglutida para o paciente, além de desencadear reações imunológicas mais graves. A liberação de novas versões da semaglutida depende, sobretudo, da comprovação de que esses riscos estão controlados.